|
 |
МАСС-СПЕКТРОМЕТРИЯ С ИНДУКТИВНО
|  |
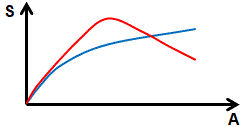
МЕТОДЫ АНАЛИЗА В МАСС-СПЕКТРОМЕТРИИ С ИНДУКТИВНО СВЯЗАННОЙ ПЛАЗМОЙГрадуировка по стандартамПринципиально количественный анализ в масс-спектрометрии с индуктивно связанной плазмой при градуировке по стандартным образцам не отличается от количественного анализа в других спектральных методах. Калибровочный график представляет собой зависимость интенсивности сигнала, полученного при измерении стандарта, от концентрации аналита в этом стандарте. Естественно, что последовательная градуировка прибора стандартами, содержащими один элемент, при проведении многоэлементного анализа займет намного больше времени, чем калибровка по стандарту, содержащему все необходимые элементы. По этой причине для градуировки прибора, как правило, используют многоэлементные стандарты. Существует ряд логических ограничений на состав многоэлементных стандартов. Во-первых, в одном стандарте не должны содержаться элементы, создающие изобарные наложения друг на друга. Во-вторых, следует учитывать возможность взаимодействия элементов друг с другом, в результате чего могут получаться нерастворимые соединения. Популярный набор стандартов High Purity состоит из трех растворов, состав которых приведен ниже. Стандарт А: Al, As, Ba, Be, Bi, B, Ca, Cd, Ce, Co, Cr, Cs, Cu, Dy, Er, Eu, Ga, Gd, Ho, In, Fe, La, Pb, Li, Lu, Mg, Mn, Nd, Ni, P, K, Pr, Re, Rb, Sm, Sc, Se, Na, Sr, Tb, Tl, Th, Tm, U, V, Yb, Y, Zn (2% HNO3); Стандарт В: Sb, Ge, Hf, Mo, Nb, Si, Ag, Ta, Te, Sn, Ti, W, Zr (2% HNO3 + следы HF); Стандарт С: Au, Ir, Os, Pd, Pt, Rh, Ru (2% HNO3 + следы HCl). Отличительной особенностью масс-спектрометрии с индуктивно связанной плазмой является широкий диапазон линейности калибровки. Линейность градуировочного графика сохраняется в пределах до 5 и более порядков концентрации в зависимости от выбранного изотопа и условий измерения. Построив градуировочный график, выходящий из нуля по единственному стандарту с концентрацией, например, 10 мкг/л, можно не жертвуя точностью анализа определять концентрацию этого элемента от 2 до 50 мкг/л. Зачастую, можно без ущерба для точности определения работать с градуировкой по одной точке в диапазоне плюс-минус порядок от концентрации калибровочного стандарта. Основным недостатком градуировки по стандартам является то, что при определении содержания элементов не учитывается влияние неспектральных интерференций – дрейфа чувствительности прибора и матричный эффект. Для устранения влияния матрицы ее можно добавлять в градуировочные стандарты в количестве, сходном с исследуемыми образцами. Естественно, что добавляемая матрица не должна содержать значительного количества определяемых элементов. Для коррекции матричного эффекта и дрейфа прибора можно эффективно использовать внутренний стандарт (см. ниже). Метод внутреннего стандартаКоличественное определение аналитов с использованием внутреннего стандарта очень популярно в масс-спектрометрии с индуктивно связанной плазмой. В большинстве случаев метод позволяет достаточно точно учитывать влияние неспектральных интерференций на результат анализа. Одним из основных достоинств метода является его простота. Сущность метода заключается в том, что к исследуемому и контрольному образцу добавляют известное количество элемента, не содержащегося в образце. Измеряют сигнал внутреннего стандарта в контрольном образце (I0) и в образце неизвестного состава (I1). Если исследуемый образец содержит минеральную матрицу, которая подавляет сигнал, I1 будет меньше I0, поскольку контрольный образец не содержит матрицы. Для коррекции матричных влияний рассчитывают коэффициент, и умножают интенсивности сигналов аналитов на этот коэффициент для получения скорректированного значения сигнала. Внутренний стандарт должен быть близким к аналиту по физико-химическим свойствам (атомной массе, потенциалу ионизации и др.). Сильное различие этих параметров повлечет ощутимое изменение чувствительности прибора по стандарту по сравнению с аналитом. Так, например, не совсем корректной будет поправка концентрации 7Li по внутреннему стандарту 115In в силу того, что матричный эффект, связанный с формированием объемного заряда за скиммером, может по-разному влиять на чувствительность спектрометра на легких и средних массах. Близость потенциалов ионизации (ЕI1) внутреннего стандарта и аналита тоже важна, поскольку элементы с высоким ЕI1 более чувствительны к изменениям условий в плазме по сравнению с другими элементами. Например, использования скандия (ЕI1 = 6,6 эВ) в качестве внутреннего стандарта для определения цинка (ЕI1 = 9,4 эВ), мышьяка (ЕI1 = 9,8 эВ), селена (ЕI1 = 9,8 эВ) будет далеко не лучшим решением, несмотря на близость атомных масс. Для точного анализа используют несколько внутренних стандартов, привязывая к ним разные определяемые элементы, исходя из вышеизложенных соображений. На практике, особенно при анализе проб с богатым и изменяющимся качественным составом выбор внутренних стандартов является трудной задачей. По этой причине зачастую приходится идти на компромисс, используя 1-2 стандарта, и жертвуя точностью учета матричных влияний. Полуколичественный анализПолуколичественный анализ позволяет определять концентрации элементов в пробе без использования градуировочных стандартов. Для квадрупольных масс-спектрометров с индуктивно связанной плазмой имеет место взаимосвязь величины сигнала изотопа элемента с его атомной массой и потенциалом ионизации. Мерой такой взаимосвязи является так называемый коэффициент относительной чувствительности (КОЧ, relative sensitivity factor, RSF). Коэффициент относительной чувствительности вычисляется по следующему соотношению: КОЧ = I × M / (c × A × E × NA) где: I – интенсивность сигнала (имп/сек); M – молярная масса элемента; с – массовая концентрация элемента в растворе; A – содержание целевого изотопа; E – энергия ионизации; NA – число Авогадро. Для разных спектрометров характерен разный вид зависимости чувствительности от атомной массы изотопа – кривая чувствительности спектрометра (Рис. 1).
Рис. 1. Виды зависимости чувствительности (S) квадрупольных масс-спектрометров с индуктивно связанной плазмой от атомной массы (А) измеряемого изотопа. По кривой чувствительности, построенной по трем-четырем изотопам во всем диапазоне масс, можно достаточно точно определить чувствительность спектрометра по изотопам, не включенным в градуировку, а, следовательно, можно рассчитать их концентрацию, измерив сигнал. Однако следует учитывать, что элементы с высоким потенциалом ионизации выпадают из типичной зависимости, поэтому необходимо корректировать сигнал с использованием КОЧ. По такому алгоритму работает метод полуколичественного анализа в масс-спектрометрии с индуктивно связанной плазмой. В градуировочном растворе достаточно иметь 3-5 элементов во всем диапазоне масс, чтобы построить кривую чувствительности и количественно определить весь перечень элементов. При полуколичественном анализе допускается использование внутреннего стандарта. Ошибка полуколичественного анализа достаточно велика и может достигать 50%. Кроме того, влияние интерференций на результат полуколичественного анализа гораздо более заметно, по сравнению с градуировкой по стандартам. Однако, этот прием в некоторых случаях позволяет получать результаты, практически совпадающие с полученными при использовании обычной градуировки. Полуколичественный анализ весьма эффективен для экпресс-определения содержания аналитов в пробе с целью принятия решения о дальнейших манипуляциях с ней. Метод добавокДля реализации этого метода образец делят на несколько частей, минимум на две. Ко всем частям кроме одной прибавляют ступенчато возрастающее количество аналита. Оптимальное количество образцов с добавкой составляет 2–3, при этом количество добавки должно в разы превышать ожидаемую концентрацию аналита в образце. На практике, раствор, с помощью которого производится добавка, должен быть более чем в 100 раз концентрированнее образца во избежание получения больших объемов пробы и, как следствие, ошибок, связанных с разбавлением. Полученную серию образцов измеряют и строят зависимость интенсивности сигнала каждого образца от количества добавки. Истинную концентрацию аналита в исходном образце находят как модуль величины в точке пересечения прямой с осью абсцисс. Следует помнить, что найденное значение необходимо скорректировать в соответствии с разбавлением, если таковое имело место при внесении добавки в образец. Метод добавок позволяет учесть матричные влияния, поскольку определение добавки производится из того же раствора, что и определение аналита. Фактически этот подход равносилен градуировке по стандартам на сходной матрице. Метод добавок не учитывает спектральные наложения. Их коррекцию нужно проводить отдельно. Основное ограничение метода добавок состоит в том, что при определении широкого перечня элементов в широком диапазоне концентраций внесение добавки становится весьма трудоемкой операцией. Кроме того, в разы возрастает количество анализируемых проб. Метод изотопного разбавленияМетод изотопного разбавления является самым точным способом определения содержания элементов в масс-спектрометрии с индуктивно связанной плазмой. На точность анализа с применением этого метода не оказывают влияние неспектральные интерференции, связанные с изменением чувствительности прибора во времени, матричные эффекты и т.д., поскольку измеряется не абсолютная концентрация изотопа, а изотопное отношение (см. ниже). Суть метода заключается в следующем: образец с неизвестным содержанием элементов смешивается с точным количеством добавки с известной концентрацией изотопов определяемого элемента. При этом изотопный состав добавки должен быть измененным по отношению к анализируемому образцу. В идеальном случае добавка должна быть обогащена по наименее распространенному изотопу определяемого элемента. С целью обеспечения изотопного обмена между образцом и добавкой, последнюю следует вводить на стадии разложения образца, если таковое проводится. В других случаях форма, в которой элемент существует в добавке, должна по возможности быть идентичной форме элемента в образце. Измеряют изотопные отношения (см. ниже) элемента в образце до и после введения добавки. Концентрацию элемента образце рассчитывают исходя из измеренных изотопных отношений до и после введения добавки, известного отношения изотопов в добавке и ее количества. Метод изотопного разбавления реализован в программном обеспечении всех масс-спектрометров с индуктивно связанной плазмой. Метод не чувствителен к матричным влияниям по той же причине, что и для метода добавок. Ошибки разбавления после внесения добавки также не оказывают существенного влияния на точность результатов, поскольку в этом методе измеряется не величина концентрации, а изотопное отношение. Изотопное разбавление имеет ряд ограничений: во-первых, определяемый элемент должен иметь как минимум 2 изотопа, во-вторых, эти изотопы должны быть свободны от спектральных интерференций. Кроме того, стандарты с аттестованным изотопным составом дороги и не всегда доступны. Измерение изотопных отношенийТочное определение изотопных отношений представляет собой достаточно сложную задачу. Получение правильных результатов требует не только тщательной настройки прибора (ионная оптика, мертвое время детектора и т.д.) и параметров анализа (времени интегрирования, общей статистики сбора данных), но и проведения последующих расчетов с целью внесения поправки на эффект дискриминации масс (mass bias). Дискриминация масс имеет место во всех ИСП-МС и обусловлена целым рядом факторов. Эффект выражается в понижении чувствительности спектрометра при переходе от более тяжелых изотопов к более легким. Таким образом, два изотопа одного и того же элемента в одинаковой концентрации будут давать в приборе разный по интенсивности сигнал. Подробное описание этого явления и способов его коррекции в изотопном анализе можно найти в литературе [5]. Расчет изотопных отношений осуществляется по интенсивностям сигналов соответствующих изотопов, скорректированных на эффект дискриминации масс: a = I1 / I2 × В где: I1 – интенсивность сигнала изотопа 1 (имп/сек); I2 – интенсивность сигнала изотопа 2 (имп/сек); В – коэффициент поправки на эффект дискриминации масс. Здесь показан наиболее простой способ коррекции эффекта дискриминации масс, основанный на использовании метода внешнего стандарта. Сущность метода заключается в том, что перед измерением образца измеряют стандарт с известным изотопным отношением. Коэффициент В рассчитывают следующим образом: В = Ic1 / Ic2 × ac где: Ic1 – интенсивность сигнала изотопа 1 в аттестованном образце; Ic2 – интенсивность сигнала изотопа 2 в аттестованном образце; ac – аттестованное значение изотопного отношения. Для более точного определения изотопных отношений применяются другие методы, некоторые из которых описаны в рекомендованной литературе. Измерение сигнала во времениМасс-спектрометры с индуктивно связанной плазмой позволяют регистрировать изменение сигналов выбранных изотопов во времени. Это свойство используется для прямого анализа твердых объектов с применением лазерного пробоотбора, а также при использовании ИСП-МС в качестве детектора для хроматографических методов разделения. Высокая скорость сканирования современных масс-спектрометров с ИСП позволяет измерять сигнал для десятков изотопов с хорошим временным разрешением. Программное обеспечение к ИСП-масс-спектрометрам позволяет проводить обработку данных временной зависимости сигнала. В арсенале программного обеспечения присутствует возможность интегрирования хроматографических пиков, нормирования и внутренней стандартизации сигнала. Измерение наночастицКвадрупольный масс-спектрометр с индуктивно связанной плазмой может быть использован для определения концентрации и распределения наночастиц по размерам. Попадая в плазму, твердая наночастица в силу крайне малого размера успевает полностью превратиться в ионы. Отсюда следует название метода на английском языке – single particle ICP-MS (SP-ICP-MS). Современная электроника сделала квадрупольные ИСП-МС достаточно быстрыми для того, чтобы регистрировать очень кратковременные сигналы. При коротком времени интегрирования (меньше 1 мс) спектрометр успевает зарегистрировать интенсивный пик от попавшей в плазму наночастицы. Количество пиков в течение определенного времени пропорционально концентрации наночастиц в растворе, а интенсивность пика пропорциональна размеру наночастицы. Градуировку прибора проводят по стандартному образцу наночастиц с известной концентрацией и распределением по размерам. При этом одновременно можно проводить и анализ наночастиц и определение концентрации элемента в растворе. Программное обеспечение ведущих производителей масс-спектрометров с индуктивно связанной плазмой имеет возможность проведения подобных анализов. Для получения хорошо разрешенных пиков измерения проводят из сильно разбавленных растворов. Следует учитывать, что в силу очень короткого импульса, генерируемого наночастицей, даже при очень коротком времени интегрирования удается зарегистрировать не более 3-4-х полноценных сигналов изотопов. Отсюда следует ограничение метода SP-ICP-MS в плане количества элементов, определяемых в наночастице, будь то основные элементы или примеси. | |||||
| Copyright © 2009 |